Introdução:
As dispersões químicas, isto é, as misturas de um soluto em um solvente, podem ser classificadas como: soluções verdadeiras, suspensões e coloides (ou suspensões coloidais).
O que difere de uma para a outra é o tamanho das partículas dispersas. As partículas do soluto dispersas em uma solução verdadeira são iguais ou menores que 1 nm, por isso, são misturas homogêneas e mesmo olhando em um microscópio só podemos ver uma fase. Além disso, essa mistura não pode ser separada por meio de métodos físicos, como a filtração, pois suas partículas não são retidas por um filtro e nem por uma membrana semipermeável. Um exemplo de solução é a água com sal.
As suspensões são soluções heterogêneas, dessa forma, ao misturarmos o soluto no solvente, as partículas do soluto ficam em suspensão por um pouco e logo depois se depositam no fundo do recipiente. Suas partículas possuem o tamanho maior que 1000 nm e são facilmente separadas por técnicas físicas. Um exemplo de suspensão é a mistura areia com água.
As suspensões coloidais oucoloides são aquelas que a olho nu parecem ser homogêneas, mas que ao microscópio percebemos que são na verdade heterogêneas. Suas partículas ficam suspensas na solução, não se depositam no fundo pela ação da gravidade e seu tamanho fica entre 1 nm e 1000 nm. A sua separação se dá por meio de uma membrana semipermeável. Um exemplo de coloide é o leite.
Mas, uma característica que distingue bem esses três tipos de dispersões é o seu efeito sob ação de um feixe de luz. As soluções são transparentes, as suspensões são opacas e nos coloides ocorre o chamado efeito Tyndall, que é o reflexo da luz. Isso significa que quando um feixe de luz, num ambiente escuro, atravessa um coloide ou uma suspensão, sua trajetória fica visível.
Essa propriedade será usada no experimento a seguir a fim de classificar três dispersões químicas.
Materiais e reagentes:
-
3 béqueres iguais;
-
Laser;
-
Amido de milho;
-
Sal de cozinha;
-
Gelatina sem sabor;
-
Água;
-
Cartolina preta;
-
Tesoura.
Procedimento Experimental:
Você irá preparar três soluções diferentes em cada béquer. No primeiro béquer, coloque 200 mL de água morna, dissolva uma colher de gelatina sem sabor e deixe atingir a temperatura ambiente. No segundo béquer, misture 200 mL de água em temperatura ambiente com uma colher de sal. E no terceiro, misture 200 mL de água em temperatura ambiente com uma colher de amido.
Não pare agora... Tem mais depois da publicidade ;)
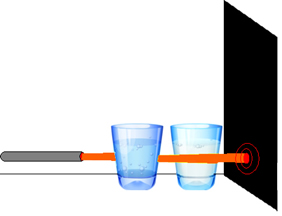
Corte a cartolina preta num tamanho de cerca de 10 cm2 e coloque-a em pé sobre uma parede. Posicione os béqueres um na frente do outro e mire com o laser, acendendo o feixe e fazendo a luz atravessar as soluções até chegar à cartolina preta. Observe o que ocorre.
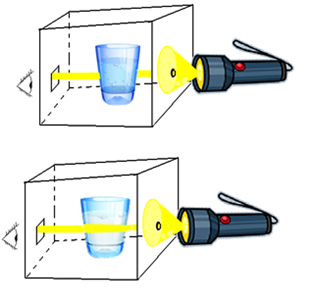
Se você não conseguir um apontador a laser com feixe de luz bem estreito, faça o seguinte: no lugar da cartolina, você usará uma caixa de papelão. Faça um pequeno buraco de um dos lados da caixa correspondente à metade da altura do béquer. E do outro lado, na mesma altura, recorte um pequeno quadrado.
Coloque um dos béqueres com uma das soluções lá dentro e feche bem a caixa. Você irá posicionar uma lanterna acesa na frente do buraco pequeno, de modo que um estreito feixe de luz passe pelo buraco e atravesse a dispersão. Você olhará do outro lado, no quadrado recortado, a fim de visualizar o que ocorreu.
Repita o mesmo processo para cada uma das dispersões.
Resultados e Discussão:
Depois de apresentar os resultados obtidos, o professor poderá pedir para que os alunos classifiquem as três dispersões utilizadas nesse experimento em solução, coloide ou suspensão.
Em seguida, promova um confronto de opiniões para que cada aluno construa seu conhecimento a partir dos dados obtidos na atividade experimental e consiga explicar por que é possível visualizar a trajetória do feixe de luz em um coloide e não é possível obter o mesmo resultado em uma solução.
Peça também para que os alunos ordenem o tamanho das partículas dispersas em ordem crescente.
Se o professor desejar, poderá usar também outros materiais comuns no cotidiano, como refrigerantes, sucos, gelatinas, geleias, entre outros.
Por Jennifer Fogaça
Graduada em Química









